资本市场又向医疗器械企业开了一道口子。
2022年6月,《上海证券交易所科创板发行上市审核规则适用指引第7号——医疗器械企业适用第五套上市标准》(下称《指引》)发布。这套上市标准不要求企业盈利,甚至不要求企业有收入,但在研发情况和估值水平上提出了较高的要求。
医疗器械企业受此青睐,与其市场潜力密不可分。数据显示,预计到2023年,中国医疗器械的市场规模将突破万亿元。
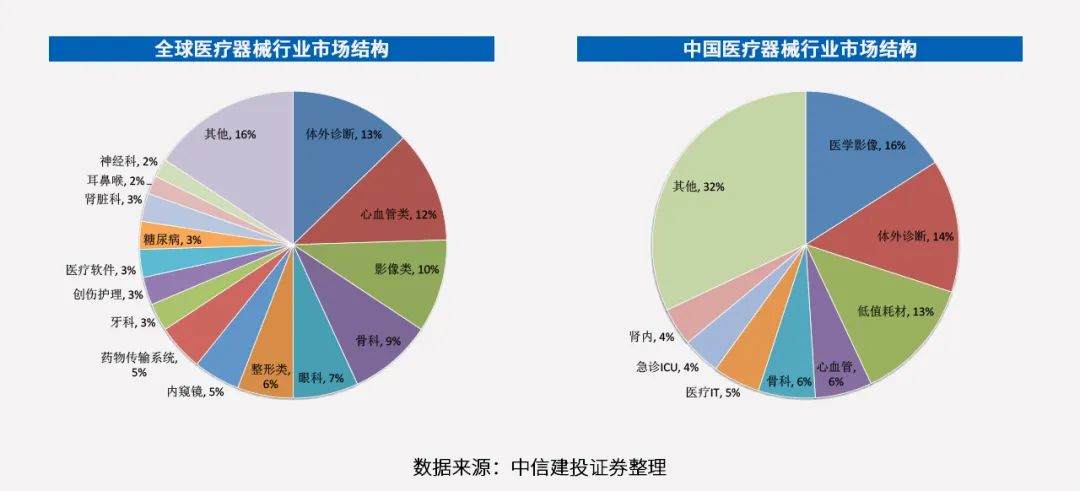
对比来看,2020年,全球医疗器械行业市场规模为4774亿美元,同比增长5.63%;中国医疗器械市场规模约为7341亿元,同比增长18.3%。也就是说,全球医疗器械市场的规模是中国的4倍多,而中国医疗器械市场的增速是全球的近4倍。目前,中国已成为仅次于美国的全球*大医疗器械市场。
除了资本市场的政策,医疗器械作为医疗健康的分支之一,受国家医药部门诸多政策的影响,尤其是集采、DRG/DIP支付等。叠加新冠疫情、国际形势等因素,医疗器械市场近几年可谓风云变幻。
过去十余年,九鼎投资在医疗器械领域投资了大量优秀企业,包括专注于眼健康和近视防控业务的欧普康视(300595)、医用导管供应商维力医疗(603309)、医用内窥镜器械和光学产品供应商海泰新光(688677)、体外诊断试剂和仪器供应商伊普诺康(835852)等。
本期「九鼎投资观察」,我们将结合医疗器械领域面临的集采、DRG/DIP支付等医疗政策,以及近期资本市场上市新规,尝试拨开医疗器械市场的迷雾,在不确定中寻找确定性。
01
集采降价温和,但仍影响商业模式、市场格局与市场规模
2017年1月,国务院发布的《“十三五”深化医药卫生体制改革规划》提到,要完善药品和高值医用耗材集中采购制度。
所谓集采,即以公立医疗机构作为集中采购主体,约定药品或医疗器械的采购量,并利用团购效应和企业进行谈判议价。集采的目的非常明确,通过降低药品或医疗器械的价格,减轻患者负担,节约医保基金的支出。
自2018年至今,药品领域已开展了七批国家集采,医疗器械领域将开展第三批国家集采。除了*集采,化学发光类IVD(体外诊断产品)、药物球囊、神经介入等医疗器械品类,也已在各省市或联盟试点进行。
2020年11月,作为医疗器械品种的全国首采,铬合金载药冠脉支架(即心脏支架,一种心血管介入耗材)集采启动。11家企业26款支架产品无分组竞价,最终10款支架产品中选,支架价格从均价1.3万元左右降至700元左右。与2019年相比,相同企业的相同产品平均降价93%。
2021年9月,国家医保局又组织开展了骨科耗材领域的人工关节集采,髋关节平均价格从3.5万元下降至7000元左右,膝关节平均价格从3.2万元下降至5000元左右,平均降价82%。
2022年7月,《国家组织骨科脊柱类耗材集中带量采购公告》发布,脊柱类耗材将成为继冠脉支架、人工关节后的第三批进行国家集采的高值耗材品种。
据国新办介绍,前六批药品集采平均降价53%。结合冠脉支架和人工关节的集采降价幅度,看起来医疗器械的集采降价幅度比药品大得多。但据我们观察,医疗器械的集采整体上会比药品温和。
从应用场景来看,大多数医疗器械从生产厂家到终端患者,中间有一个环节无法避免:伴随服务,包括提供合规的“跟台”服务、协助组装工具、必要的工具使用指导、手术操作培训等。
国家首轮集采将冠脉支架流通的中间利润环节都剥掉后,在服务流程上曾出现伴随服务缺失、影响医疗器械使用的情况。汲取此经验后,在人工关节集采时,伴随服务成了一个独立的报价单元。从集采结果来看,人工关节集采的平均降幅相比冠脉支架小了11%,这或是主要原因。
而且,不同于冠脉支架,人工关节和和脊柱类耗材的集采,均设定了多个拟中选规则(含“复活”机制)。这传递出来的信号是:中标不再唯低价论,而是更加理性。
尽管降价温和,但集采还是会对相关品种的商业模式、市场格局、市场规模等方面带来影响。
从商业模式上来说,中标与否直接影响未来企业整体的品牌推广和市场销售,因为除了集采产品,其他产品也能通过集采打通的入院渠道增加市场覆盖面。而相关品种原来以代理为主的销售模式,在集采后会较大程度改变。
从市场格局上来说,集采会对相关品种的市场格局带来局部变动,而非颠覆性洗牌。
在已经开展的人工关节集采中,同一产品系统类别下,根据医疗机构采购需求(即样本医院在集采前根据过往年度采购量进行申报,称为“报量”)、企业供应能力、产品材质(如类型和材料),将企业分单元分别竞价。
在即将开展的脊柱类耗材集采中,也综合考虑了医疗机构需求、企业供应意愿和供应能力、产品组合完整度等因素,将企业分单元分别竞价。
此举在较大程度上尊重了既有市场格局,避免出现价格引起的极端情况,保证行业的供应能力(如小企业以低价中标,但无法保证供应)。
而局部变动的点在于,集采都有一定淘汰率,而过去市场份额较高、降价意愿更强的公司将优先获得相关市场份额。按照脊柱类耗材集采规则,产品部件齐全的龙头公司,也有望获得更大优势。
至于集采对于市场规模的影响,我们认为,不同品种的情况并不相同。
对于渗透率较高的品种而言,很难通过放量来弥补降价,市场规模缩水是必然的。但对于发展阶段没那么成熟的品种而言,通过集采可以快速放量,并弥补降价带来的损失,市场规模得到增长。
02
创新和出海将成未来发展主题,真实需求和付费意愿是关键
随着集采常态化进行,接下来哪些细分领域还将纳入全国集采范围?
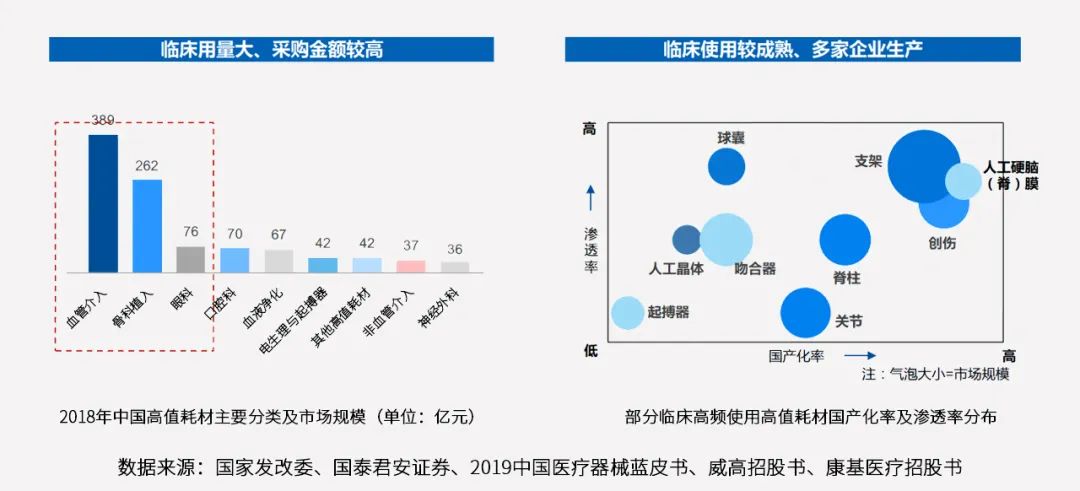
2019年7月国务院办公厅印发的《治理高值医用耗材改革方案》指出,对于临床用量较大、采购金额较高、临床使用较成熟、多家企业生产的高值医用耗材,按类别探索集中采购。
结合这一方案和已经开展的集采项目,行业普遍认为,占医保支出越高、国产化率越高的品类,被集采的概率越高。
除了集采,中国医药企业还面临的一项重要政策是:DRG/DIP支付。
2021年底,国家医保局部署了《DRG/DIP支付方式改革三年行动计划》,到2024年底,全国所有统筹地区全部开展DRG/DIP支付方式改革工作,到2025年底,DRG/DIP支付方式覆盖所有符合条件的开展住院服务的医疗机构。
DRG和DIP支付,分别为按疾病诊断相关分组付费和按病种分值付费。过去,中国的基本医疗保险支付方式主要是按服务项目付费、按服务单元付费、按人头付费、按单病种付费等。
和集采类似,DRG/DIP支付的推行是为了提高医保基金使用效率、控制医疗费用不合理上涨。
对于中国医疗器械企业而言,随着冠脉支架、人工关节等细分领域逐渐转向红海,以及集采常态化和DRG/DIP付费模式推行,其在本土市场的盈利空间会逐渐收缩。在此背景下,他们该如何应对?
一方面,医疗器械企业可通过在非集采的品类中进行产品创新,来获得部分产品的高溢价和利润率。
例如,在2020年开展的冠脉支架国家集采中,乐普医疗的钴基合金雷帕霉素洗脱支架系统中标。乐普医疗表示,随着国家组织冠脉支架集中带量采购的实施,传统金属药物支架经营业务显著下降,但该公司的介入创新产品组合(可降解支架、药物球囊、切割球囊等)在2021年的营业收入同比增长 827.36%。
赛诺医疗旗下的BuMA冠脉药物洗脱支架为不锈钢材质,未参与国家集采。该公司也在公开渠道称,支架耗材类需要多种规格才能满足不同病变部位病人的临床需求。随着临床手术量的增加,未来非集采的产品仍存在较大空间。
需要指出的是,医疗器械是多学科交叉的领域,涉及光学、物理、生物化学、精密机械、计算机硬件软件等。创新需依托于这些学科的进步,很难做0~1的创新,更多是在已有产品的基础上做一些微创新或微改良。这也需要从业人员、资本和监管有更多耐心,尊重学科规律,理性看待周期。
一般而言,医疗器械的微创新从这几个方面进行:
精确度或灵敏度的创新,如提高诊断试剂的灵敏度。
简便性的创新,以缩短流程、减少时间。
商业模式的创新,如在面向医院端的产品上,研发家用或商用的创新产品。
我们认为,企业不能为了创新而创新。我们做投资价值判断时,并不关心单个技术的好坏。只有能满足真实需求的技术进步才意味着付费意愿,才是有价值的。
另一方面,和许多其他行业类似,医疗器械的出海也是重要的机会。
中国加入世界贸易组织(WTO)已超20年,对外开放的步调不会停下。海外巨头不断入华,国内企业也需要走向世界。而且,如前文所述,全球医疗器械的市场规模是中国的4倍有余,可为中国企业带来新的增长点。
据了解,目前很多中国企业计划建立国际化平台,在前期以防疫物资出口开拓的国际市场的基础上,通过设立海外分公司或汇集国内企业资源抱团出海,进一步拓展海外市场渠道。
此外,也有许多企业将“一带一路”沿线国家和地区作为海外市场拓展重点,还有一些技术门槛较高的细分领域企业,选择与欧美等发达国家和地区企业开展研发和销售渠道上的合作。
03
上市新规利好“硬科技”企业,投资价值需结合多因素综合判断
分析了行业基本面,我们再回过头来看资本市场的规则。
时间回到2019年初,上交所发布了《关于就设立科创板并试点注册制相关配套业务规则公开征求意见的通知》,明确发行人申请股票*发行上市的,应当至少符合五项上市标准中的一项。
其中,科创板第五套上市标准,是指“预计市值不低于人民币40亿元,主要业务或产品需经国家有关部门批准,市场空间大,目前已取得阶段性成果。医药行业企业需至少有一项核心产品获准开展二期临床试验,其他符合科创板定位的企业需具备明显的技术优势并满足相应条件”。
自2019年7月科创板开板后的三年时间里,适用第五套标准上市的企业基本是生物创新药公司,未见医疗器械企业成功案例,因医疗器械企业适用第五套标准的申报操作细不明确,企业申报和监管审核实质判断的难度都较大。
鉴于这种不确定性,很多未盈利的医疗器械企业选择香港上市或改道以科创板*套标准上市。
直到2022年3月,微创医疗旗下专注于电生理介入诊疗与消融治疗的医疗器械企业——微创电生理,成功“吃到螃蟹”,作为首家医疗器械企业以科创板第五套成功过会。
有了实践案例和可参照的模板,上交所顺势推出了上述《指引》。
我们认为,《指引》对医疗器械和投资行业来说,整体利好。未盈利但科创属性强的医疗器械企业登陆科创板有法可依,上市确定性更强。
我们也判断,新政会吸引一批未盈利医疗器械企业到科创板上市,但不会扎堆。
从《指引》相关内容来看,对申请适用科创板第五套上市标准的医疗器械企业作出了细化规定:
比如,核心技术产品应当属于国家医疗器械科技创新战略和相关产业政策鼓励支持的范畴;核心技术产品研发应当取得阶段性成果;主要业务或产品市场空间大;具备明显的技术优势等。
这些规定加上第五套上市标准中的市值要求,就排除了很多医疗器械企业。
而满足科创板第5套上市标准的医疗器械公司,大多已经在港交所上市或排队上市。我们看到,自2018年港交所向未盈利生物科技公司开闸后,目前有超过50家未盈利生物科技公司在港交所上市,其中医疗器械企业仅10余家。
科创板还给企业设置了一个隐性门槛:连续两年扣非净利润为负,且营业收入低于1 亿元,将会面临退市风险。科创板在审评企业的IPO申请时,会根据此“盈利时间表”,来倒推企业当前的业务能力。若判断企业在两年后会有退市风险,IPO申请将不能通过。
2022年7月29日,《公开发行证券的公司信息披露编报规则第25号——从事药品及医疗器械业务的公司招股说明书内容与格式指引》公布并开始施行。该文件正式指出,拟公开发行证券的公司,预计未盈利状态持续存在或累计未弥补亏损继续扩大的,应分析触发退市条件的可能性,并充分披露相关风险。
综合而言,我们认为,《指引》利好“硬科技”企业的发展,但对于投资机构的投资决策不会有太大的影响。企业是否值得投资,最终要根据它的科技含量、市场地位、行业空间、发展周期和面临的风险,来判断其基本面和内涵价值。
随着经济发展和医疗需求升级,以及港股18A和A股注册制推行,中国医疗器械行业和创新药类似,进入了新的发展周期——资本充沛,各种新技术、新公司不断涌现,百花齐放、热闹非凡。
从单个细分赛道来看,我们关注集中度的提升。例如全国骨科脊柱类产品带量采购落地后,我们预计,该行业的集中度将进一步提升,国产龙头公司有望获得较高的市场份额。因此,在骨科赛道中,我们更关注产品管线齐全、研发实力较强、且拥有一定品牌力的核心竞争力企业。
从创新的角度来看,我们认为,一些新型高附加值的低值耗材也存在较好的投资机会。例如根据我们的调研,可吸收免打结的医用缝合线,单价*值不高,但消耗量大,且在医保报销范围内,现在在临床上很受欢迎。
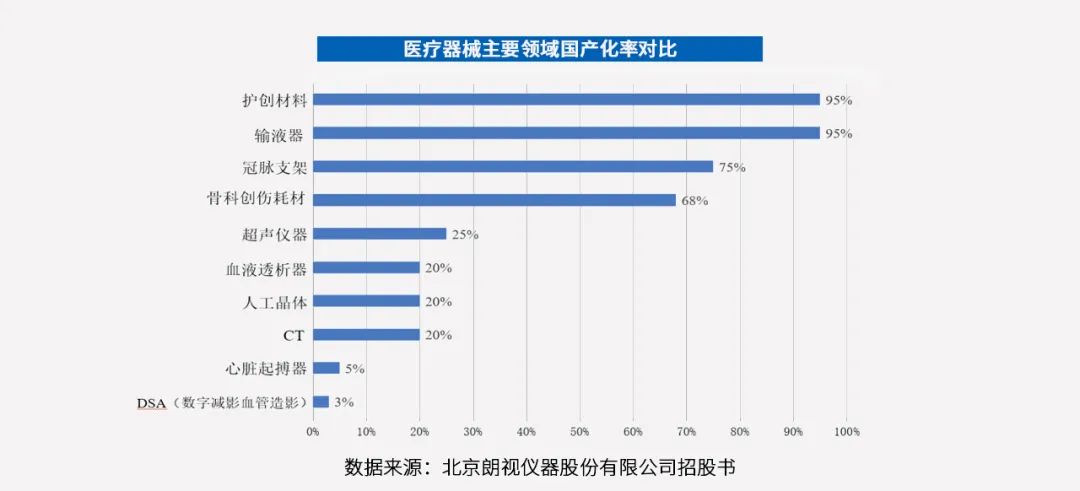
从长期成长性的角度来看,国产化率或可作为一个判断标准。我们认为,20%的国产化率是一个拐点。这个数值以上,医疗器械国产化进展迅速,会逐渐出现上市公司。因此,在一级市场,国产化率20%~50%的细分领域,如神经介入、心脏介入、肿瘤介入、骨科运动医学、吻合器等,具备较大的投资机会。
作为医疗器械的重要分支,IVD也是我们长期关注的细分领域。对此,我们在一文中已有阐述。
另外,我们也关注医疗器械领域CMO/CDMO(生产服务外包)的投资机会。过去,有规模化销量的医疗器械很少,生产环节基本是厂家自己做。但我们观察到,近年医疗器械领域开始出现了代工模型。未来随着医疗器械规模化上量,这一领域的CMO/CDMO将具备较大发展潜力。
免责声明:本网站内容主要来自原创、合作伙伴供稿和第三方自媒体作者投稿,凡在本网站出现的信息,均仅供参考。本网站将尽力确保所提供信息的准确性及可靠性,但不保证有关资料的准确性及可靠性,读者在使用前请进一步核实,并对任何自主决定的行为负责。本网站对有关资料所引致的错误、不确或遗漏,概不负任何法律责任。任何单位或个人认为本网站中的网页或链接内容可能涉嫌侵犯其知识产权或存在不实内容时,应及时向本网站提出书面权利通知或不实情况说明,并提供身份证明、权属证明及详细侵权或不实情况证明。本网站在收到上述法律文件后,将会依法尽快联系相关文章源头核实,沟通删除相关内容或断开相关链接。



